Page 120 -
P. 120
При взаимодействии с водой щелочные металлы образуют
щелочь, выделяя водород: 2Na + 2H O = 2NaOH + H
(тв.) 2 (ж.) (водн) 2(г.)
Рубидий и цезий взаимодействуют со льдом при низкой
ПРОЕКТНАЯ ВЕРСИЯ
температуре (–110 ˚С).
Области применения щелочных металлов и их соединений
разнообразны. Высокая химическая активность щелочных ме-
таллов, их способность к взаимодействию с компонентами воз-
духа используются для удаления пузырьков воздуха из сплавов
и создания вакуума в электроприборах. Щелочные металлы
Все права принадлежат АОО "Назарбаев Интеллектуальные школы"
применяются для создания сплавов с другими металлами, на-
пример, сплавы натрия с ртутью (амальгамы) используются для
извлечения золота. Современные щелочные аккумуляторы по-
строены на основе гидроксида лития. С древних времён соеди-
нения натрия и калия использовались как моющие средства.
ВОПРОСЫ И ЗАДАНИЯ
1. В марте 2019 года в г. Дубне (РФ) состоялся запуск ускорительного комплекса для синтеза новых
химических элементов. Учёные надеются синтезировать первый элемент восьмого периода – эле-
мент № 119. Назови свойства данного элемента, сравнив его с францием: электронная формула
внешнего уровня, радиус, электроотрицательность, металлические или неметаллические свойства,
химическая активность.
2. С какими из следующих веществ: кислород, азот, фтор, вода, растворы гидроксида натрия, хло-
рида лития, серной кислоты – будет взаимодействовать калий? Запиши уравнения возможных
реакций, назови продукты взаимодействия. Какие из реакций являются окислительно-восстано-
вительными? Почему?
3. Осуществи превращения по схеме: Na→NaOH→Na SO . Назови вещества.
2 4
4. Определи два химических элемента, расположенных по соседству в Периодической системе
химических элементов Д. И. Менделеева. В соединениях они проявляют степень окисления (+1).
Соединения одного из них окрашивают пламя в жёлтый цвет, другого – в фиолетовый.
5. В трёх пронумерованных пробирках находятся растворы хлоридов лития, натрия и калия. Опре-
дели содержимое пробирок, не используя другие реактивы.
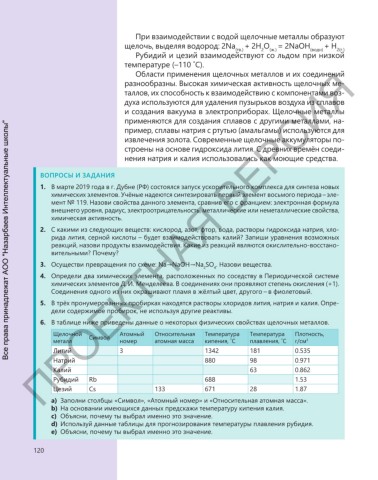
6. В таблице ниже приведены данные о некоторых физических свойствах щелочных металлов.
Щелочной Символ Атомный Относительная Температура Температура Плотность,
металл номер атомная масса кипения, ˚С плавления, ˚С г/см 3
Литий 3 1342 181 0.535
Натрий 880 98 0.971
Калий 63 0.862
Рубидий Rb 688 1.53
Цезий Cs 133 671 28 1.87
a) Заполни столбцы «Символ», «Атомный номер» и «Относительная атомная масса».
b) На основании имеющихся данных предскажи температуру кипения калия.
с) Объясни, почему ты выбрал именно это значение.
d) Используй данные таблицы для прогнозирования температуры плавления рубидия.
е) Объясни, почему ты выбрал именно это значение.
120